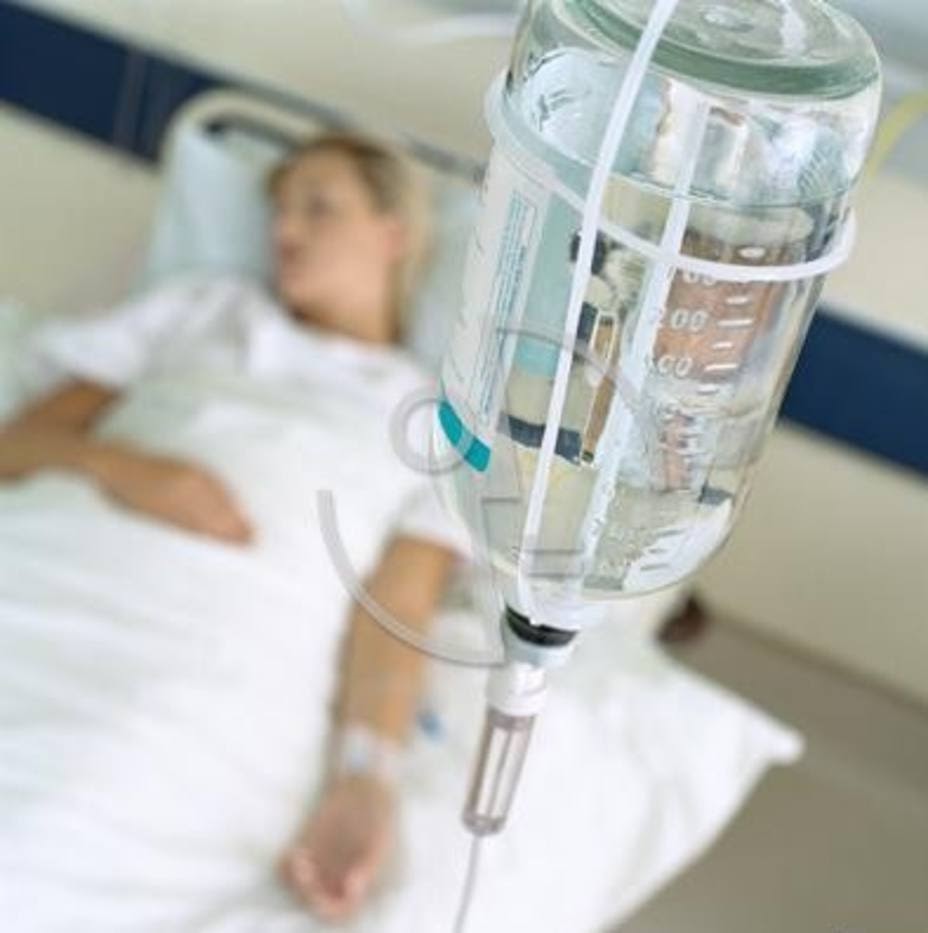
¿QUÉ SON? Son preparados líquidos, estériles que contienen una o varias sustancias disueltas, como electrolitos, nutrientes o fármacos, en un solvente o mezcla apropiada de solventes miscibles entre sí, que se le administra a un paciente en distintas situaciones de salud, mediante el sistema de infusión continua o por medio del torrente sanguíneo.

El objetivo de su administración puede ser el de mantenimiento de las pérdidas de agua y electrólitos durante condiciones fisiológicas normales como la orina, respiración, sudoración y heces; y la expansión del volumen intravascular en estados de depleción de volumen con compartimento extravascular disminuido (diarrea, vómito, hemorragia, etc.), y compartimiento extravascular aumentado (sepsis, pancreatitis, cirugía, quemaduras, cirrosis e insuficiencia cardíaca), con la finalidad de mejorar el gasto cardíaco y la perfusión tisular o microcirculatoria.
Las soluciones parenterales se pueden clasificar según su peso molecular en:
- Cristaloides: Soluciones iónicas, de fácil difusión a través de una membrana semipermeable, que contiene agua, electrolitos, y azúcares en distintas proporciones, pudiendo ser por lo tanto Hipotónicas, Isotónicas o Hipertónicas según su concentración respecto al plasma.
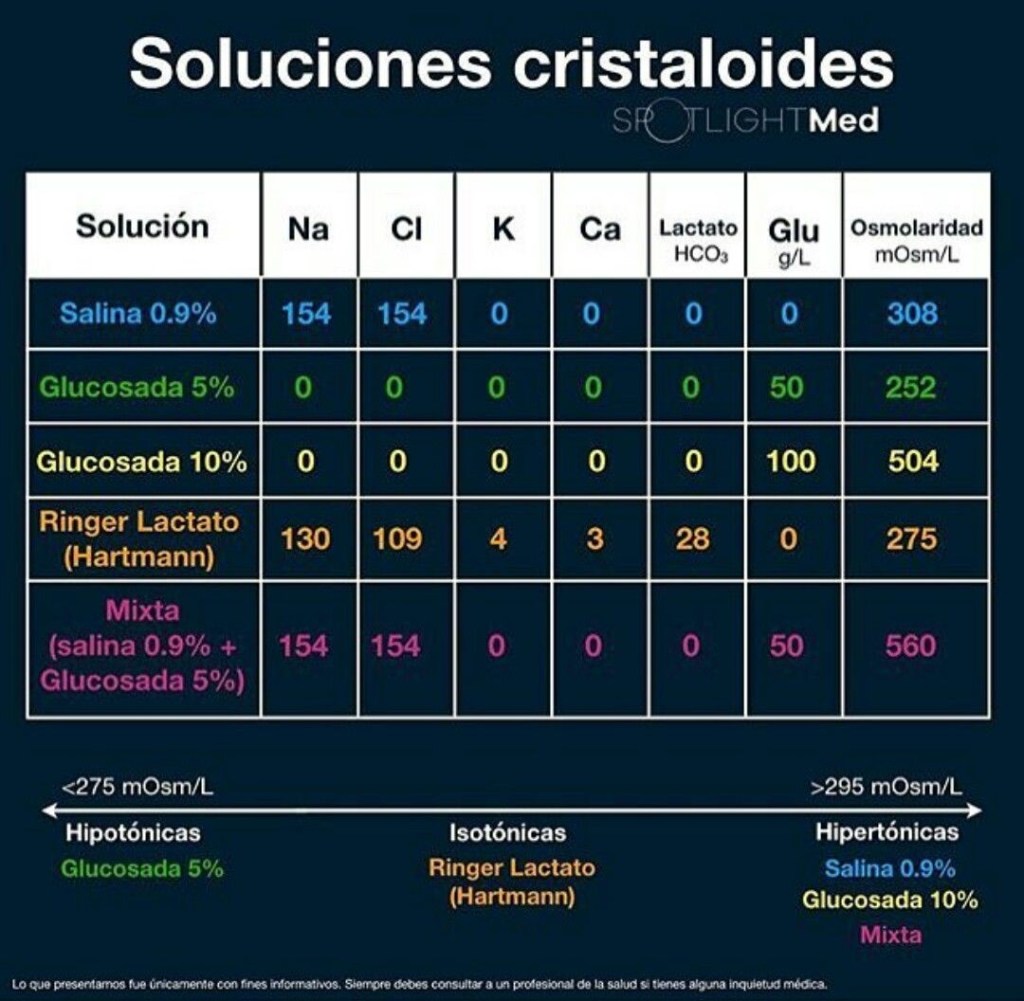
Cristaloides Hipotónicas
Una solución hipotónica es una solución que contiene menos soluto que la célula que se coloca en ella. Se definen también como soluciones que tienen una osmolaridad menor a la del plasma (menor de 280 mOsmol/l).
Se usan para corregir anomalías electrolíticas como la hipernatremia, por pérdida de agua libre en pacientes diabéticos o con deshidratación crónica, donde prima la pérdida de volumen intracelular.
Si una célula con una concentración de NaCl se coloca en una solución de agua destilada, que es agua pura sin sustancias disueltas, la solución en el exterior de la célula es 100% de agua y 0% de NaCl. Dentro de la célula, la solución es 99,1% de agua y 0,9% de NaCL. El agua, de nuevo, va de una concentración más alta a una concentración más baja para disolver la concentración de soluto para alcanzar el equilibrio. Así que el agua va desde la solución de agua destilada hasta el interior de la célula para diluir la concentración de soluto dentro de la célula.
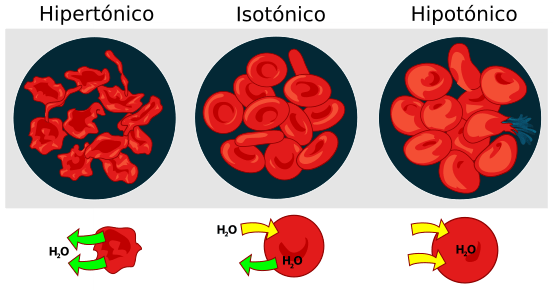
Cristaloides Hipertónicas
Una solución hipertónica es una solución que contiene más soluto que la célula que se coloca en ella. La solución hipertónica tiene mayor osmolaridad que el plasma (superior a 300 mOsmol/L) y mayor concentración de sodio.
Si se coloca una célula con una concentración de NaCl de 0,9% en una solución de agua con una concentración de NaCl al 10%, se dice que la solución es hipertónica.
Cuando la solución contiene más soluto, esto significa que contiene menos agua. La solución fuera de la célula es 10% de NaCl, lo que significa que es 90% de agua. La solución dentro de la célula es 0,9% de NaCl, lo que significa que es 99,1% de agua. La solución fluye de una mayor concentración de agua a una menor concentración de agua. Esto es para diluir las áreas de mayores concentraciones de soluto, por lo que se puede alcanzar el equilibrio. Siendo que la solución exterior es 90% de agua mientras que el interior contiene 99,1% de agua, el agua fluye desde el interior de la célula a la solución exterior para diluir las áreas altas de concentración de soluto. Por lo tanto, la célula pierde agua y se encoge.
Cristaloides Isotónicos
Una solución isotónica es una solución en la que la misma cantidad de soluto y solución está disponible dentro de la célula y fuera de la célula. Una solución isotónica tiene una osmolaridad similar a la del plasma, entre 272 300 mOsmol/litro.
La solución y el porcentaje de soluto son los mismos dentro de la célula que en la solución fuera de la célula. Por lo tanto, usando los números anteriores, una célula colocada en una solución de agua con NaCl al 0,9% está en equilibrio. Así, la célula permanece del mismo tamaño. La solución es isotónica en relación con la célula.
Los líquidos isotónicos se utilizan para hidratar el compartimiento intravascular en situaciones de perdida de líquido importante, como deshidratación, hemorragias, etc. Se necesita administrar entre 3 y 4 veces el volumen perdido para lograr la reposición de los parámetros hemodinámicos deseados.
Coloides:
- Solución de alto peso molecular que no atraviesa las membranas capilares, siendo capaces de esta forma de aumentar la presión osmótica plasmática y retener agua en el espacio intravascular. Por este motivo son conocidos como expansores plasmáticos
- Coloides naturales
- Coloides artificiales


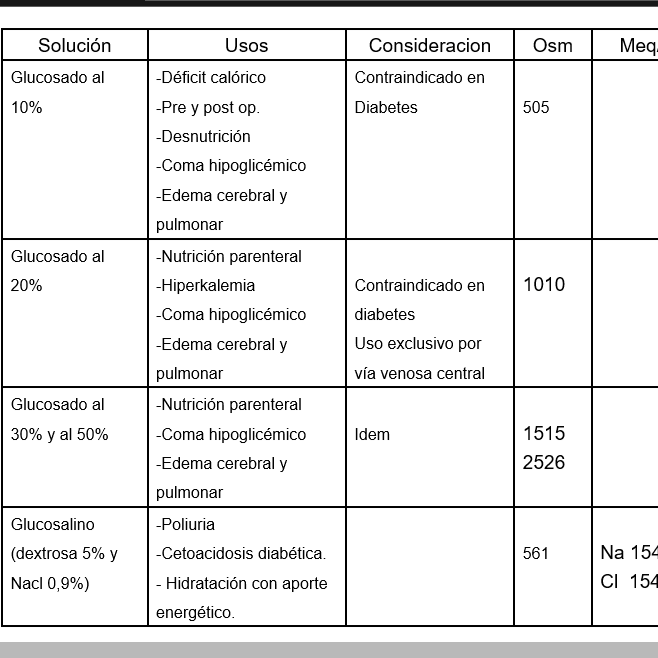
TIPOS DE SOLUCIONES CRISTALOIDES:
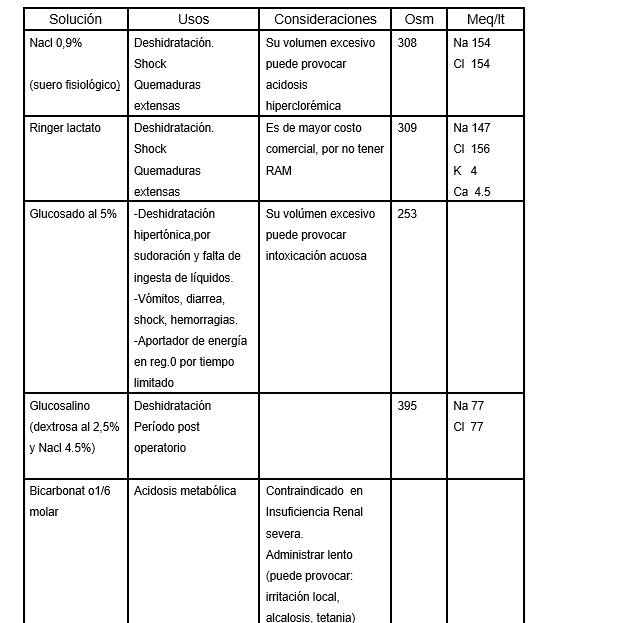
- Solución Salina Normal (SSN 0,9%)
La solución salina normal al 0,9% también denominada suero fisiológico, es la sustancia cristaloide estándar, es levemente hipertónica respecto al líquido extracelular y tiene un pH ácido.
La relación de concentración de sodio (Na) y de Cloro (Cl.) que es 1/1 en el suero fisiológico, es favorable para el sodio respecto al cloro (3/2) en el líquido extracelular (Na+ mayor Cl). La normalización del déficit de la volemia es posible con la solución salina normal, aceptando la necesidad de grandes cantidades, debido a la libre difusión entre el espacio vascular e intersticial de esta solución. No es químicamente normal, pero tiene gran utilidad en la mayoría de las situaciones en las que es necesario realizar repleción de líquidos corporales, y es de bajo costo. Muchos la prefieren como solución rutinaria de combate. Sin embargo, si se prefunden cantidades no controladas, el excedente de cloro del líquido extracelular desplaza los bicarbonatos dando lugar a una acidosis hiperclorémica.
- Lactato de Ringer o Solución de Hartmann
Esta solución isotónica contiene 51 mEq/L de cloro menos que la SSN, generando sólo hipercloremia transitoria, por lo que tiene menos posibilidad de causar acidosis.
Por ello, se utiliza de preferencia cuando se deben administrar cantidades masivas de soluciones cristaloides. Se considera que es una solución electrolítica balanceada en la que parte del sodio de la solución salina isotónica es reemplazada por calcio y potasio.
La proporción de sus componentes le supone una osmolaridad de 272 mOsmol/L. El efecto de volumen que se consigue es muy similar al de la solución salina normal. La vida media del lactato plasmático es de más o menos 20 minutos, pudiéndose ver incrementado este tiempo a 4 6 horas en pacientes con shock.
El lactato es una solución alcalótica que contiene 130 mEq/L de sodio, 109 mEq/L de cloro y 28 mEq/L de lactato, unión que es convertida por el hígado en bicarbonato y por ello se utiliza en estados de acidosis.
- Dextrosa en Agua Destilada al 5% (DAD 5%)
Es una solución hipotónica de glucosa, cuyas dos indicaciones principales son la rehidratación en las deshidrataciones hipertónicas y como agente portador de energía.
Proporciona un aporte calórico significativo. Cada litro de solución glucosada al 5% aporta 50 gramos de glucosa, que equivale a cerca de 200 Kcal. Este aporte calórico reduce el catabolismo proteico, y actúa por otra parte como productor de combustible de los tejidos del organismo más necesitados (sistema nervioso central y miocardio).
Entre las contraindicaciones principales se encuentran las situaciones que puedan conducir a un cuadro grave de intoxicación acuosa por una sobrecarga desmesurada y pacientes con Enfermedad de Adisson en los cuales se puede producir una crisis por edema celular e intoxicación acuosa.
Coloides
Los coloides son fluidos de reemplazo de la sangre anormalmente perdida, del plasma u otros fluidos extracelulares. El término coloide se refiere a aquellas soluciones cuya presión oncótica es similar a la del plasma. Las soluciones coloidales contienen partículas en suspensión de alto peso molecular que no atraviesan las membranas capilares, de forma que son capaces de aumentar la presión osmótica plasmática y retener agua en el espacio intravascular.
Los coloides se clasifican en naturales y artificiales. Dentro de los naturales se encuentra la albúmina y las fracciones proteicas del plasma y entre los artificiales se destacan los dextranos, hidroxietilalmidones y las gelatinas.
El tiempo de duración de los coloides es directamente proporcional al tamaño de las partículas que lo componen y su necesidad varía según la patología.
Solución coloide ideal
La solución de coloide ideal es aquella que esté libre de reacciones alérgicas e infecciosas, ejerza una presión osmótica intravascular sostenida, fácil almacenamiento, y además tenga costo reducido. Ninguna de las soluciones que se disponen en la actualidad cumple todas estas características.

Hay cuatro tipos de coloides disponibles para uso clínico, y han sido desarrollados y utilizados como expansores del espacio intravascular, basado en la compresión de la Ley de Starling.
Coloides naturales
También llamados coloides derivados del plasma, son todos preparados de la sangre o plasma donada, tienen riesgo de transmisión de infecciones.
Albumina
Es la proteína predominante del plasma y aporta cerca del 75 al 80% de la presión coloido-osmótica. La albúmina es una solución monodispersa, con un peso molecular promedio de 69.000 Daltons y pH fisiológico.
La función de la albúmina en la sangre consiste en mantener la presión oncótica normal, transportar distintas sustancias, inactivar pequeños grupos de compuestos (disulfirán, lípidos, eicosanoides, etc.), actuar como tampón plasmático, mantener la integridad microvascular y poseer acción antioxidante puesto que inhiben la formación de radicales libres de oxigeno de los polimorfo nucleares.
La concentración de electrolitos que posee esta en rango fisiológico, asemejándose en este sentido a las soluciones salinas isotónicas. Además, la albúmina al 5% produce una presión oncótica próxima a la del plasma. Su permanencia en el espacio vascular es de 24 horas. Aproximadamente 10% de la albúmina es destruida en el organismo diariamente.
Coloides artificiales
Los coloides sintéticos son suspensiones con moléculas de tamaños y pesos moleculares diferentes. Las sustancias más usadas son las gelatinas, los dextranos y los almidones.
Dextranos
Son polímeros de glucosa de diferente peso molecular que son producidos por la bacteria “leuconostoc mesenteroides”, cuando crecen en un medio azucarado. Hay dos tipos de dextranos, el 70% y el 40%. La molécula del dextrán o dextrano es un polisacárido monocuaternario de origen bacteriano. Las principales soluciones disponibles son de PM promedio de 70.000, 60.000 o 40.000 Da.
Su eliminación se realiza fundamentalmente por vía renal. Son hiperoncóticas y promueven tras su infusión una expansión de volumen del espacio intravascular por medio de la afluencia del líquido intersticial al vascular. El dextrán tiene propiedades antitrombóticas importantes, al alterar la adhesividad plaquetaria y deprimir la actividad del factor VIII.
Dentro de las complicaciones se encuentra la falla renal aguda, anafilaxia y diátesis hemorrágica.
Gelatinas
Las gelatinas son obtenidas por degradación del colágeno de origen animal. A través de diversos procesos es posible obtener gelatinas fluídas modificadas o gelatinas con puentes de urea, ambas con PM promedios de 35.000 Da.
Su poder oncótico es menor a la albúmina y su vida media en el intravascular relativamente corta, de 2 a 3 horas, siendo eliminadas rápidamente por filtración glomerular. Asociado a la escasa incidencia de efectos a nivel renal o de la coagulación, permite que no haya dosis límites establecidas para las gelatinas.
Hidroxietilalmidones
Los almidones son polímeros naturales de glucosa derivados de la amilopectina, generalmente provenientes del maíz o trigo. Las soluciones de almidón natural son muy inestables en el plasma al ser rápidamente metabolizadas por las amilasas. La hidroxietilación o esterificación en diversas posiciones de la molécula permite retardar esta hidrólisis confiriéndole una gran estabilidad a la solución. Los almidones más estables y usados en clínica son los hidroxietilalmidones.
El peso molecular promedio es de 450.000 Daltons con un rango entre 1.000 y 3’000.000 lo que hace que su eliminación sea muy lenta. La vida media de los almidones hidroxietílicos en el espacio plasmático es mayor, disminuyendo después de 24 a 36 horas por excreción renal de las moléculas pequeñas y por acción de la amilasa.
La administración de los almidones hidroxietílicos se ha asociado con reacciones alérgicas (incidencia de 0.085%) y alteraciones de la hemostasia. Aumento en el Tiempo de Protrombina, Tiempo Parcial de Tromboplastina y Tiempo de Sangría, además de disminución de niveles de factor VIII. Los almidones hidroxietílicos alteran inicialmente la coagulación por hemodilución, y luego acelerando la conversión de fibrina en fibrinógeno causando formación de trombo menos estable, educiendo la actividad del factor VIII y alterando la agregación plaquetaria.